Hay una pastilla que se vende en el supermercado, junto a las vitaminas y los probióticos, con la que la gente duerme más tranquila —en todos los sentidos de la expresión— porque es «natural». Esa pastilla es la melatonina. Y si llevas tiempo tomando melatonina cada noche, merece la pena que leas esto.
No vengo a asustar. Vengo a contextualizar.
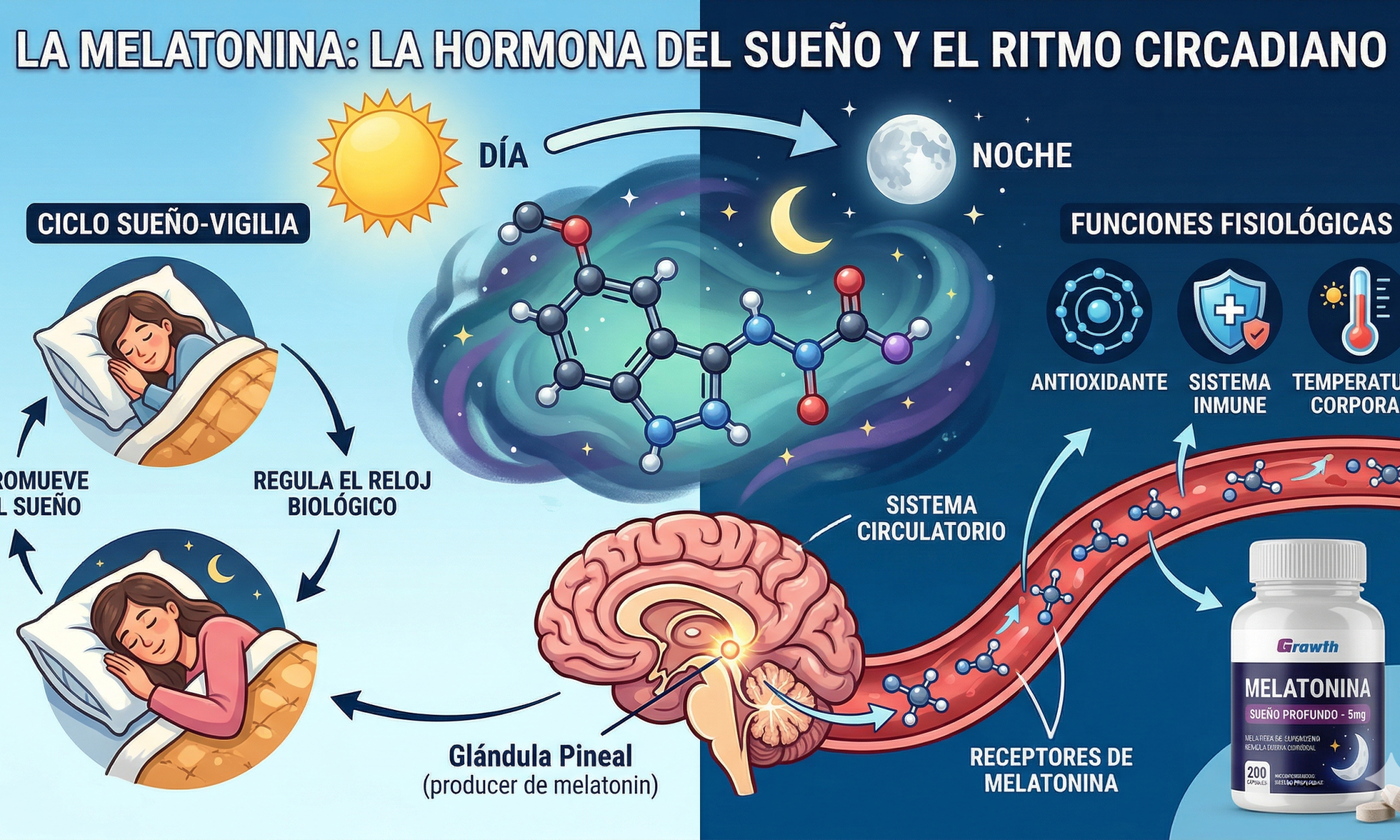
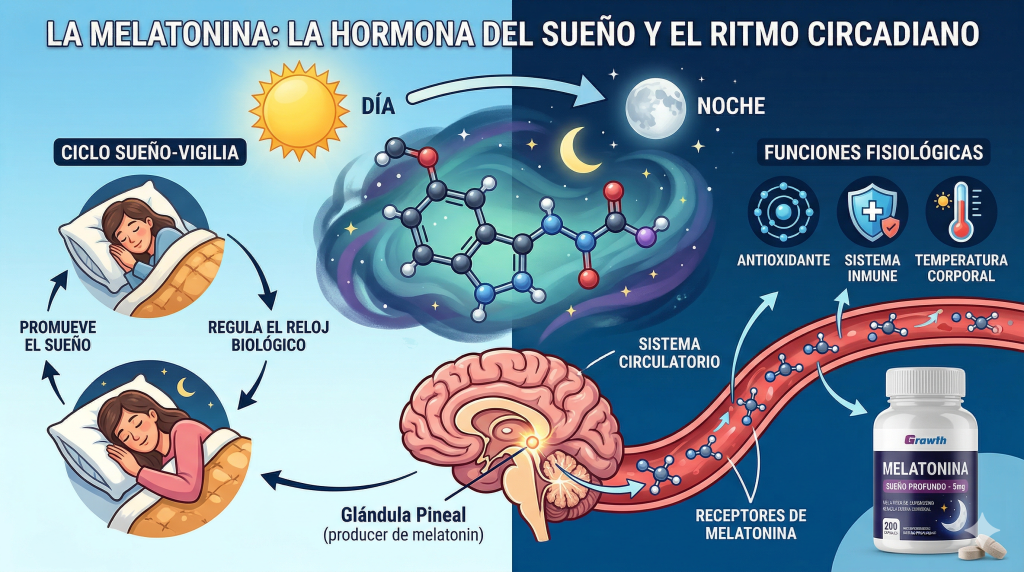
Melatonina cada noche: lo que produce tu cuerpo y lo que te metes
Tu glándula pineal fabrica melatonina de noche, en un rango que raramente supera los 60 picogramos por mililitro de sangre. Es una señal hormonal muy precisa, casi un susurro: «oye, sistema, que se está haciendo de noche». No es un somnífero. Es una señal de sincronización.
Existe además una preocupación a largo plazo sobre la propia glándula. La calcificación pineal —un proceso degenerativo activo, no un simple desgaste— reduce de forma proporcional la capacidad de producción de melatonina endógena: a mayor grado de calcificación, menores niveles de 6-sulfatoximelatonina urinaria, que es el marcador habitual de la función pineal. Lo que investigan algunos grupos es si la suplementación crónica, al suprimir la actividad metabólica de la glándula por retroalimentación negativa, podría acelerar ese proceso de atrofia por desuso. La evidencia histológica en humanos no es todavía concluyente, pero la posibilidad de transformar una deficiencia relativa en una permanente es razón suficiente para no tomar este suplemento indefinidamente sin ningún tipo de control.
Un factor que empieza a recibir atención en este contexto es el fluoruro. La glándula pineal es el órgano con mayor concentración de fluoruro del cuerpo humano, por dos razones estructurales: está fuera de la barrera hematoencefálica —lo que permite el paso libre del ión— y tiene el mayor contenido de hidroxiapatita de cualquier tejido blando, con alta afinidad por el fluoruro. Estudios en cadáveres han documentado concentraciones de fluoruro en la pineal superiores a las del hueso, con una correlación positiva entre fluoruro y calcificación (r=0,73). La hipótesis es que el fluoruro acumulado interfiere con enzimas clave de la síntesis de melatonina, particularmente la arilalquilamina N-acetiltransferasa (AA-NAT). No es una hipótesis marginal: hay investigación publicada en revistas indexadas respaldándola, y estudios poblacionales canadienses y estadounidenses han encontrado asociación entre exposición crónica al fluoruro en agua y alteraciones del sueño. El debate sobre los umbrales de seguridad de la fluoración del agua está abierto: en 2024, un informe del Programa Nacional de Toxicología de EE.UU. concluyó con confianza moderada que exposiciones elevadas de fluoruro se asocian con menor cociente intelectual en niños, y ese mismo año un tribunal federal ordenó a la EPA revisar formalmente la evidencia. Si la preocupación por el fluoruro en la pineal tiene o no relevancia clínica a los niveles habituales de fluoración, es algo que la investigación todavía no ha resuelto. Pero es un debate que existe, que tiene base, y que conviene conocer.

El problema es lo que venden en las farmacias. La dosis más común comercializada oscila entre 1 y 10 mg. Eso puede elevar tus niveles plasmáticos entre 10 y 100 veces por encima del pico fisiológico máximo. Es como si alguien susurra «buenas noches» y tú le pones un altavoz de concierto. El mensaje llega, sí. Pero algo más también se entera.
Además, la biodisponibilidad oral de la melatonina es extremadamente variable: entre el 1% y el 37% según cada persona. Eso significa que dos individuos tomando la misma pastilla pueden tener respuestas completamente distintas, lo que explica por qué algunos duermen como troncos y otros no notan nada… y entonces doblan la dosis. Mal asunto.
Los datos de 2025
En noviembre de 2025, en las Sesiones Científicas de la American Heart Association, se presentaron los datos de un análisis de más de 130.000 adultos con insomnio. Bien diseñado, con emparejamiento estadístico para controlar variables de confusión. Los resultados no eran exactamente tranquilizadores.
Los usuarios crónicos de melatonina —más de doce meses— mostraron un riesgo un 89% mayor de desarrollar insuficiencia cardíaca. La probabilidad de hospitalización por esa causa fue casi tres veces y media superior. Y la mortalidad por cualquier causa se duplicó.
¿Es un estudio observacional? Sí. ¿Establece causalidad definitiva? No. ¿Deberíamos ignorarlo porque no encaja con el relato del suplemento inocuo? Tampoco. La robustez de los datos tras los análisis de sensibilidad hace que los mecanismos biológicos propuestos sean plausibles: alteración del tono simpático cardíaco, interacciones con otros fármacos a través del citocromo CYP1A2, efectos paradójicos sobre la regulación autonómica a largo plazo.
En cardiología no hay suplementos inocentes. Solo suplementos sobre los que todavía no hay suficientes datos. Y en este caso, los datos ya empiezan a llegar.
Tu sistema hormonal no es un interruptor de luz
La melatonina no actúa solo en el sueño. Es un integrador neuroendocrino. Se comunica con el eje hipotálamo-hipófisis-gonadal (el que regula la reproducción y la pubertad) y con el eje hipotálamo-hipófisis-adrenal (el del cortisol y la respuesta al estrés).
En pediatría, esto tiene implicaciones que ya no son solo teóricas. En mamíferos, la bajada de melatonina es la señal que activa el inicio de la pubertad. Mantener niveles elevados de forma artificial puede retrasar esa maduración. Hay estudios observacionales que apuntan en esa dirección, incluyendo uno longitudinal que documentó posibles retrasos tras tratamientos de más de siete años.
El impacto potencial en el esqueleto en desarrollo añade otra capa de precaución. La melatonina tiene efectos complejos sobre osteoblastos y osteoclastos que en el adulto pueden ser protectores, pero en el hueso inmaduro la evidencia experimental sugiere que dosis elevadas podrían interferir con la homeostasis del cartílago de crecimiento. La clínica en humanos es todavía emergente y contradictoria, lo que no significa que el riesgo sea descartable: significa que estamos interviniendo hormonalmente en ventanas críticas del desarrollo sin saber aún con exactitud qué consecuencias tiene esa intervención. Eso, por sí solo, debería llevar a extremar la precaución en niños.
En adultos con burnout o agotamiento crónico, el uso indiscriminado puede aplanar la curva matutina de cortisol —esa que necesitas para arrancar el día— y enmascarar una disfunción del eje HPA sin corregirla. Es decir: te sientes dormido por la noche, pero el problema de fondo sigue ahí, solo que ahora tienes un parche encima que impide verlo.
Hay un tercer sistema al que se presta menos atención: el inmune. La melatonina es un inmunomodulador activo que estimula la producción de citoquinas proinflamatorias —IL-1, IL-2, IL-6, TNF-α— y favorece una respuesta tipo Th1. En personas sanas eso es irrelevante. En personas con enfermedades autoinmunes activas puede no serlo. En la artritis reumatoide, por ejemplo, los niveles nocturnos elevados de melatonina endógena ya se asocian con la rigidez matutina característica de la enfermedad; hay mecanismo propuesto y algo de evidencia directa de que la melatonina estimula la proliferación de células sinoviales y la producción local de citoquinas inflamatorias en la articulación. En lupus y esclerosis múltiple la evidencia es fundamentalmente preclínica, pero el mecanismo es suficientemente plausible como para que cualquier persona con patología autoinmune activa lo consulte antes de tomar melatonina de forma habitual, y como para que el clínico lo tenga en cuenta antes de recomendarla.
Lo que hay realmente en esa cápsula
En muchos países, la melatonina se regula como suplemento dietético, no como fármaco. Eso tiene consecuencias prácticas que van más allá del debate regulatorio: análisis independientes han encontrado productos con entre un -83% y un +478% de la cantidad declarada en la etiqueta. Y variaciones de hasta el 465% entre lotes de la misma marca.
Pero lo más preocupante no es la dosis incorrecta. Es que aproximadamente el 26% de los suplementos de melatonina analizados contienen serotonina no declarada. Para alguien que toma un antidepresivo ISRS o un IMAO, eso puede desencadenar un síndrome serotoninérgico: una emergencia médica con inestabilidad autonómica, rigidez muscular e hipertermia. También se ha detectado CBD y metales pesados en algunas formulaciones en gominola, especialmente populares en población infantil.
Cuando algo no está regulado como medicamento, el control de calidad es una lotería. Y en este caso, es una lotería que se juega con los ojos cerrados.
Melatonina en la dieta: lo que los alimentos pueden y no pueden hacer
Antes de hablar de cuándo tiene sentido suplementar, conviene situar lo que la dieta puede aportar. Algunos alimentos contienen melatonina endógena, aunque en cantidades del orden de los nanogramos por gramo —es decir, entre un millón y cien mil veces menos que la dosis mínima del suplemento comercial. No estamos hablando de un efecto farmacológico; estamos hablando de una señal fisiológica coherente con lo que el organismo espera recibir a través de la alimentación.
El alimento con evidencia clínica más sólida son las cerezas ácidas (variedad Montmorency): el jugo concentrado ha demostrado en ensayos aumentar los niveles plasmáticos de melatonina y mejorar la eficiencia del sueño en adultos mayores con insomnio. Los demás alimentos de la lista —nueces, huevos, pescado azul, avena— aportan concentraciones menores de melatonina directa, pero su utilidad real pasa por otra vía: el troptófano, aminoacácido precursor que el organismo convierte en serotonina y, finalmente, en melatonina. Para que esa conversión ocurra correctamente hacen falta cofactores: vitamina B6 y magnesio. Una dieta deficiente en cualquiera de ellos limita la síntesis endógena independientemente de lo que se suplementa.
Una advertencia sobre el dato de los pistachos: circula en divulgación nutricional un valor de 233.000 ng/g procedente de un único estudio de 2019 que estudios posteriores no han podido replicar. Si esa cifra fuera correcta, un puñado de pistachos equivaldría a varios miligramos de melatonina, lo que produciría somnolencia inmediata intensa. No ocurre. El rango real que recoge la literatura es de 2 a 230 ng/g. Un buen alimento, con magnesio y B6 de bonificación; no un suplemento encubierto.
| Alimento | Contenido aproximado | Nota |
| Cerezas ácidas | 13.000–15.000 ng/g | Mayor evidencia clínica. Jugo: 120–180 ml/día. |
| Pistachos | 2–230 ng/g | Dato alto (233.000) no replicado. Buenos por B6 y magnesio. |
| Nueces | 3–4 ng/g | Elevan melatonina plasmática con ingesta regular. Antioxidantes. |
| Huevos / pescado azul | 1–1,5 ng/g | Melatonina directa y troptófano precursor. |
| Avena / cereales | 1–1,8 ng/g | Facilitan la entrada de troptófano al cerebro vía insulina. |
Una última observación que encuadra todo lo anterior: la melatonina que aporta la dieta es, en el mejor de los casos, una contribución marginal. Lo que realmente determina los niveles nocturnos es la síntesis endógena de la pineal, y esa síntesis depende críticamente de la oscuridad. La luz en el espectro azul —pantallas, LED, iluminación artificial nocturna— suprime esa producción de forma aguda e inmediata a través de las células ganglionares de la retina. Comer bien de noche y luego pasar dos horas mirando una pantalla es, en términos de señal circadiana, trabajo perdido.
¿Cuándo tiene sentido tomar melatonina cada noche?
La melatonina no es el demonio. Tiene indicaciones con evidencia sólida. El jet lag agudo, el trastorno de fase retrasada del sueño, el trastorno no-24 en personas con ceguera, y algunas situaciones específicas en trastornos del neurodesarrollo. En esos contextos sí que podemos usar melatonina cada noche (ajustando la duración según sea requerido y aporta beneficio real.
El problema es el uso masivo para el insomnio crónico inespecífico. Ahí, tanto la American Academy of Sleep Medicine como la European Sleep Research Society la desaconsejan, señalando que la reducción de la latencia del sueño frente a placebo es modesta y que los riesgos a largo plazo no están cuantificados. El insomnio crónico necesita evaluación y tratamiento real, no una pastilla de melatonina cada noche de farmacia que aplaza el problema.
Y si se usa, la dosis cronobiológicamente activa es entre 0,3 y 0,5 mg, tomada varias horas antes de dormir. No 5 mg justo antes de apagar la luz. Dosis superiores a 1 mg saturan los receptores, producen lo que se llama «resaca de melatonina» —niveles elevados que persisten durante el día siguiente—, y aumentan exponencialmente los riesgos sin mejorar el sueño.
Para terminar
La melatonina es una hormona sistémica potente disfrazada de suplemento inofensivo porque proviene de una fuente «natural». Esa narrativa tiene un coste: millones de personas tomando melatonina cada noche indefinidamente sin ningún tipo de supervisión, en dosis farmacológicas, sin saber lo que hay realmente en la cápsula, y sin que nadie les haya preguntado por qué no duermen bien.
El insomnio no es un déficit de melatonina. Es casi siempre la señal de algo: estrés crónico, higiene de sueño deficiente, disrupción circadiana por luz artificial, ansiedad no tratada, apnea del sueño… La melatonina no resuelve ninguno de esos problemas. Solo los silencia temporalmente mientras siguen haciendo su trabajo en segundo plano.
Si la estás tomando de forma puntual para reajustar tu ritmo circadiano tras un viaje o un cambio de horario, adelante. Si la tomas cada noche desde hace más de tres meses porque si no «no puedes dormir», quizás es el momento de preguntarte —o de que alguien te ayude a preguntarte— qué está pasando realmente.
Si reconoces en tu caso alguno de los patrones que hemos descrito, puedes reservar consulta aquí.
———
Nota sobre las fuentes: Este artículo integra datos del estudio de cohorte multinacional presentado en las Sesiones Científicas de la American Heart Association (noviembre 2025), guías clínicas de la AASM y la ESRS, y revisiones farmacológicas sobre biodisponibilidad, disrupción neuroendocrina y toxicología de suplementos publicadas en JCSM, PMC y revistas especializadas.